|
|
|||
|
|||
|
ГЛАВА 5
5.4. Распределение Максвелла |
|
Вид функции распределения (5.41), полученный в предыдущем параграфе с использованием принципа детального равновесия, может быть установлен и с помощью более формальных рассуждений, не связанных с исследованием особенностей взаимодействия молекул газа между собой. Рассмотренный ниже подход был предложен Максвеллом в 1859 году.
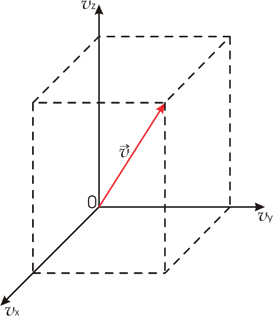
Введем пространство скоростей. Скорость 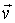 любой молекулы газа можно представить через её проекции любой молекулы газа можно представить через её проекции 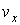 , , 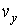 и и 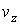 на соответствующие оси системы координат в пространстве скоростей. Если указанные значения отложить по осям на соответствующие оси системы координат в пространстве скоростей. Если указанные значения отложить по осям 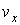 , , 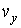 и и 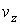 системы координат, то можно построить пространство скоростей, каждая точка в котором будет соответствовать определенному набору проекций скорости молекулы газа (см. рис. 5.3). системы координат, то можно построить пространство скоростей, каждая точка в котором будет соответствовать определенному набору проекций скорости молекулы газа (см. рис. 5.3).
Далее сделаем предположение, что вероятности попадания значений проекций скорости молекулы
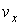 , , 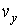 и и 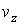 в соответствующие интервалы в соответствующие интервалы 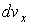 , , 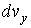 и и 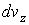 не зависят друг от друга, то есть значения проекций скорости молекул на ортогональные оси считаются статистически независимыми величинами. Тогда по аналогии с формулой (5.10) функцию распределения не зависят друг от друга, то есть значения проекций скорости молекул на ортогональные оси считаются статистически независимыми величинами. Тогда по аналогии с формулой (5.10) функцию распределения 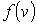 можно представить в виде: можно представить в виде:
где
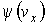 , , 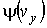 и и 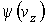 - функции распределения значений соответствующих проекций скорости - функции распределения значений соответствующих проекций скорости 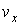 , , 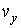 и и 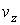 , причем вид этих функций должен быть одинаковым, так как все оси системы координат в пространстве скоростей равноправны. , причем вид этих функций должен быть одинаковым, так как все оси системы координат в пространстве скоростей равноправны.Прологарифмируем выражение (5.42):
Подстановка в него формулы, связывающей величину скорости и значения её проекций
приводит к единственно возможному выражению для функции распределения:
или
что полностью совпадает с формулой (5.41), полученной на основе применения принципа детального равновесия.
Соответственно функция распределения для значений проекций скорости
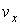 приобретает вид: приобретает вид:
Здесь константы
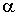 и и 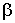 необходимо определять, исходя из условия нормировки (5.5) и значения среднего квадрата скорости хаотического движения молекул газа (2.34). необходимо определять, исходя из условия нормировки (5.5) и значения среднего квадрата скорости хаотического движения молекул газа (2.34).Введем следующие обозначения:
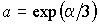 , ,
с учетом которых функция (5.47) приобретет вид:
В соответствии с условием нормировки (5.5) можно записать:
В этой формуле выбраны бесконечные пределы интегрирования. Но, конечно, реальная скорость движения молекулы не может достигать бесконечного значения, так как её величина ограничена, в частности, совершенно невероятным случаем, когда кинетическая энергия одной молекулы приближается к суммарной кинетической энергии всех молекул газа. Тем не менее, вследствие резкого уменьшения подынтегрального выражения при
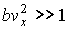 , ошибки, связанные с бесконечным выбором пределов интегрирования, оказываются достаточно малыми. , ошибки, связанные с бесконечным выбором пределов интегрирования, оказываются достаточно малыми.Для нахождения интеграла (5.50) можно использовать интеграл Пуассона:
применение которого дает
Второе условие, которое может быть использовано для нахождения неизвестных констант, является следствием определения средней кинетической энергии молекул газа через его температуру (2.42) для случая одномерного движения:
Использование правила нахождения среднего значения (5.6) дает
или с учетом формулы (5.52)
Интеграл в выражении (5.55) может быть проинтегрирован по частям с использованием интеграла Пуассона:
Подстановка получившегося выражения в (5.55) дает:
или
Соответственно коэффициент
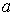 принимает вид принимает вид
Таким образом, функция распределения значений проекции скорости
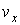 приобретает форму приобретает форму
а функция распределения скоростей молекулы газа соответственно вид
или
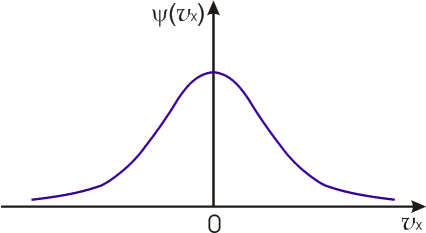
Функции (5.60) и (5.61) (или (5.62)) называются функциями распределения Максвелла. Качественно вид функции (5.60), изображенной на рис. 5.4, совпадает с нормальным законом распределения Гаусса, описывающим распределение ошибок измерений случайной величины.
Кроме полученного выше распределения Максвелла
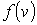 часто при проведении расчетов используется распределение по абсолютным значениям скоростей молекул газа. Для получения этого распределения запишем в общем виде вероятность того, что значения проекций скорости лежат внутри элементарного объема пространства скоростей часто при проведении расчетов используется распределение по абсолютным значениям скоростей молекул газа. Для получения этого распределения запишем в общем виде вероятность того, что значения проекций скорости лежат внутри элементарного объема пространства скоростей 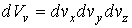 : :
Учитывая то, что эта вероятность зависит только от величины скорости и не зависит от её направления в пространстве, элементарный объем
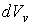 можно считать имеющим форму шарового слоя со средним радиусом можно считать имеющим форму шарового слоя со средним радиусом 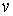 и толщиной и толщиной 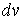 . Указанная возможность связана с тем, что в любой точке на поверхности сферы, центр которой совпадает с началом координат пространства скоростей, значения скорости . Указанная возможность связана с тем, что в любой точке на поверхности сферы, центр которой совпадает с началом координат пространства скоростей, значения скорости 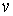 , а следовательно и функции , а следовательно и функции 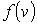 , одинаковые. Тогда элементарный объем , одинаковые. Тогда элементарный объем 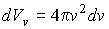 и выражение (5.63) приобретет форму: и выражение (5.63) приобретет форму:
Функция
или
называется функцией распределения Максвелла по абсолютным значениям скорости, и она показывает вероятность того, что величина скорости имеет значения от
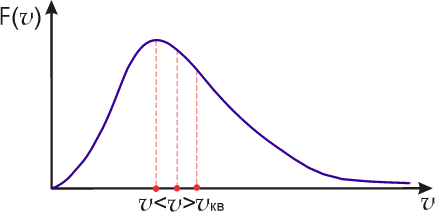
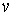 до до 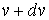 . .На рис. 5.5 изображен график функции распределения
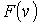 . Максимум этой функции соответствует наиболее вероятному значению скорости молекул газа . Максимум этой функции соответствует наиболее вероятному значению скорости молекул газа 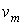 , которую можно определить, приравняв к нулю производную от функции , которую можно определить, приравняв к нулю производную от функции 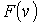 : :
Отсюда следует, что кроме случаев когда
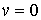 и и 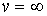 , соответствующих минимуму функции , соответствующих минимуму функции 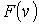 , имеется решение , имеется решение
дающее выражение для наиболее вероятной скорости молекул газа.
Кроме наиболее вероятной скорости, функция
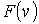 позволяет найти среднюю скорость позволяет найти среднюю скорость
и среднее значение квадрата скорости
Вычисление интегралов окончательно дает выражения для средней скорости
и для средней квадратичной скорости молекул
Формула (5.72) для средней квадратичной скорости может быть также получена на основании формулы (2.30), описывающей среднюю кинетическую энергию поступательного движения молекул газа.
Полученные значения скоростей численно отличаются друг от друга на небольшую величину, причем
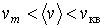 , что проиллюстрировано на рис. 5.5. , что проиллюстрировано на рис. 5.5.Кроме функции распределения по скоростям
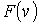 применяется функция распределения по значениям кинетической энергии поступательного движения молекул применяется функция распределения по значениям кинетической энергии поступательного движения молекул 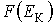 , характеризующая вероятность попадания значений кинетической энергии , характеризующая вероятность попадания значений кинетической энергии 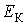 в интервал в интервал 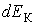 : :
Приравняв вероятности
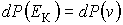 или или 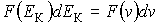 , и используя подстановку , и используя подстановку 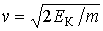 и и 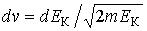 , имеем: , имеем:
В заключении отметим, что все полученные распределения справедливы только для равновесного состояния термодинамической системы. Вследствие достаточно общего метода их получения, они применимы не только для газов, но и для любых систем, движение микрочастиц которых описывается уравнениями классической механики.
Задача 5.3. Определить наиболее вероятное значение кинетической энергии поступательного движения молекул газа, находящегося в равновесном состоянии.
Решение: Определим производную функции
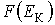 и приравняем её к нулю: и приравняем её к нулю: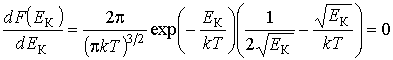 . .Тогда имеем выражение для наиболее вероятного значения кинетической энергии:
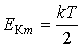 . .Из полученного выражения следует, что наиболее вероятное значение кинетической энергии поступательного движения в три раза меньше среднего значения этой энергии молекул газа.
|
|
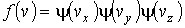 ,
,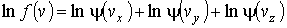 .
.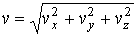 ,
,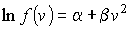
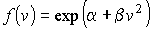 ,
,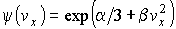 .
.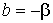 ,
,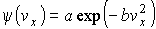 .
.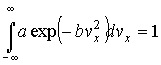 .
.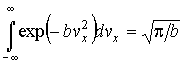 ,
,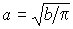 .
.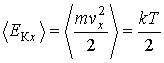 .
.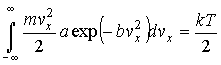 ,
,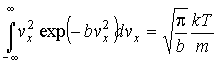 .
.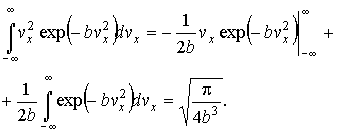
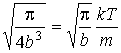 ,
,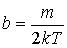 .
.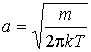 .
.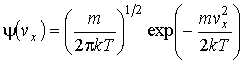 ,
,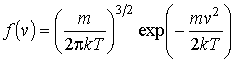
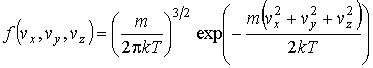 .
.
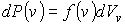 .
.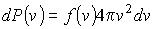 .
.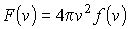
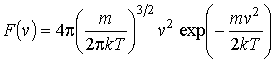
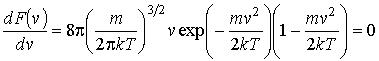 .
.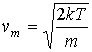 ,
,
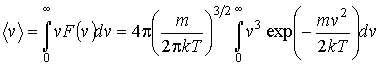
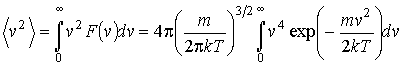 .
.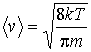
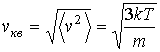 .
.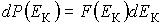 .
.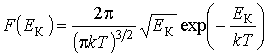 .
.