2.5. Адиабатический процесс
В параграфе 1.4 было введено понятие адиабатически изолированной системы, то есть системы, которая не обменивается теплотой с окружающими телами. Процессы, происходящие в такой системе, называются адиабатическими. Так как при адиабатических процессах  , то первое начало термодинамики для них можно записать в форме: 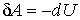 . . | (2.74) |
Совместное применение этого выражения и уравнения Клапейрона-Менделеева позволяет получить уравнение, описывающее адиабатический процесс в идеальном газе. Для этого представим выражение (2.74) в виде: 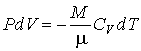 . . | (2.75) |
Нахождение полных дифференциалов от правой и левой частей уравнения Клапейрона-Менделеева (2.10) дает:  . . | (2.76) |
Вычитание из этой формулы выражения (2.75) приводит его к виду 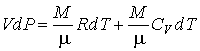 . . | (2.77) |
С учетом соотношения Майера (2.70) имеем: 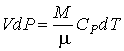 . . | (2.78) |
Умножим выражение (2.75) на отношение теплоемкостей 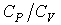 и сложим его с формулой (2.78). Тогда получим 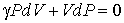 , , | (2.79) |
где введено обозначение
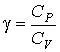 . . | (2.80) |
Величина 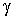 называется показателем адиабаты. Формулы (2.65) и (2.71) позволяют определить показатель адиабаты через количество степеней свободы 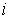 : 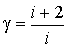 . . | (2.81) |
Из этого выражения следует, что показатель адиабаты для идеального газа всегда больше единицы. Для одноатомных газов этот показатель равен 1,67, а для двухатомных и многоатомных соответственно 1,4 и 1,33.
Поделив уравнение (2.79) на произведение  преобразуем его к виду 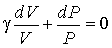 | (2.82) |
или
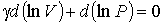 . . | (2.83) |
Отсюда следует:
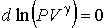 . . | (2.84) |
Интегрирование этого уравнения позволяет получить формулу
 . . | (2.85) |
которая называется уравнением Пуассона в честь французского механика, математика и физика СимеонаДени Пуассона (1781 - 1840). Это уравнение адиабатического процесса для идеального газа, или адиабаты - кривой, описываемой этим уравнением.
С помощью уравнения Клапейрона-Менделеева уравнение (2.85) можно переписать, используя другие параметры состояния идеального газа: 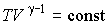 , , | (2.86) |
 . . | (2.87) |
Сравнивая уравнение Пуассона (2.85) с уравнением Бойля-Мариотта (2.11):  , можно убедиться, что адиабата идеального газа, построенная в координатах  , всегда идёт круче изотермы (см. рис. 2.6). | Рис. 2.6.
График адиабатических процессов (1) и изотермического процесса (2). |
Это связано с тем, что, как указывалось выше, показатель адиабаты для газов всегда больше единицы и принимает наибольшее значение для одноатомных газов. Поэтому самую крутую адиабату имеют инертные газы, молекулы которых состоят из одного атома.
Поскольку адиабата пересекает все изотермы данной термодинамической системы, возможен адиабатический переход с одной изотермы на другую, путём сжатия или разрежения газа. А посредством изотермического изменения объёма возможен переход с одной адиабаты на другую.
Работу идеального газа в адиабатическом процессе можно определить с помощью выражения (2.74). Интегрирование (см. комментарий к формулам (1.6) - (1.8)) этого выражения дает: 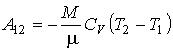 , , | (2.88) |
где: 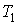 и 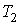 - температуры газа в начале и в конце процесса соответственно. В данном случае работа при переходе из одного состояния системы в другое определяется только функцией состояния системы 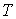 , так как путь перехода однозначно задан уравнением Пуассона. Молярная теплоемкость газа 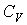 может быть выражена через показатель адиабаты 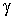 . Подстановка в формулу (2.80) соотношения Майера (2.70) приводит её к виду 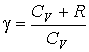 , , | (2.89) |
из которого следует искомое выражение:
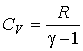 . . | (2.90) |
С учетом этой формулы выражение (2.88) может быть представлено в форме  . . | (2.91) |
На основании уравнения адиабаты (2.86) запишем соотношение между температурами и объемами газа в начальном и конечном состояниях: 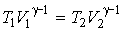 | (2.92) |
или
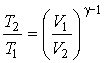 . . | (2.93) |
Подстановка этой формулы в выражение (2.91) дает 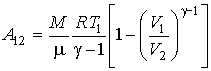 | (2.94) |
или с учетом уравнения Клапейрона-Менделеева (2.10)  . . | (2.95) |
Формула (2.95) может быть получена и непосредственно с помощью интеграла (1.13), при подстановке в него уравнения Пуассона (2.85), записанного для произвольной точки адиабаты  . . | (2.96) |
Тогда имеем
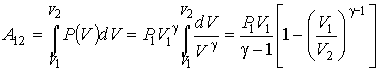 . . | (2.97) |
Адиабатический процесс может быть реализован в газе либо путём его термоизоляции, либо за счёт быстрого протекания процесса, когда процесс теплопередачи не успевает произойти. Первый способ применялся в опытах Джоуля, описанных выше, где было принципиально необходимо достижение газом состояния, близкого к равновесному. Поэтому каждый из опытов требовал продолжительного времени (около часа) и возникала необходимость введения поправок на тепловые потери.
Примером быстропротекающего процесса является распространение звука в воздухе. Несмотря на то, что такой процесс нельзя считать равновесным, опыт показывает, что для его описания возможно применение уравнения Пуассона, полученного в рамках равновесной термодинамики.
В 1816 году, за семь лет до вывода Пуассоном уравнения адиабатического процесса, Пьером Симоном Лапласом (1749 - 1827) была получена формула для скорости распространения звука в газе
 , , | (2.98) |
где: 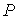 и 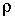 - давление и плотность газа. Измерения значений 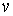 , 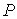 и 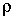 позволяют по этой формуле рассчитать значение показателя адиабаты 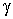 . Для воздуха это значение близко к 1,4, что указывает на возможность с хорошей точностью считать его состоящим из двухатомных молекул. Экспериментальное определение молярных теплоёмкостей  и  для реальных газов представляет собой довольно сложную задачу. Большой вклад в её решение внёс Анри Виктор Реньо (1810 - 1878), под руководством которого были измерены молярные теплоёмкости многих веществ, в том числе газов. Исследования проводились в лаборатории при Сервской фарфоровой мануфактуре и носили прикладной характер, связанный с совершенствованием тепловых машин. Некоторыми из методик, разработанных Ренье, впоследствии воспользовался Джоуль при проведении своих опытов. Задача 2.2. Внутри закрытого теплоизолированного цилиндрического сосуда находится теплонепроводящий поршень, который может двигаться без трения. В начальный момент поршень находится в середине сосуда и делит его на равные части объемом 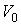 . В каждой из этих половин цилиндра находится идеальный газ с показателем адиабаты . В каждой из этих половин цилиндра находится идеальный газ с показателем адиабаты 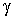 при давлении при давлении 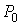 . Какую работу надо совершить, чтобы уменьшить объём одной из половин в два раза? . Какую работу надо совершить, чтобы уменьшить объём одной из половин в два раза?
Решение: В обеих частях цилиндрического сосуда будет происходить адиабатический процесс
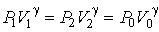 ,
где объёмы  и и  двух частей сосуда связаны соотношением двух частей сосуда связаны соотношением
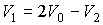 .
Пусть происходит уменьшение в два раза половины сосуда, описываемой объемом  , то есть объем , то есть объем 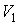 изменяется от изменяется от 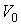 до до  . Соответственно объем . Соответственно объем 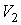 увеличивается от увеличивается от 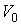 до до 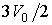 . Тогда элементарная работа, совершаемая над газом, будет определяться разностью давлений в двух частях сосуда: . Тогда элементарная работа, совершаемая над газом, будет определяться разностью давлений в двух частях сосуда:
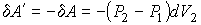 ,
где учтено, что 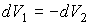 . .
Подстановка в последнюю формулу первых двух соотношений и её интегрирование дает
При 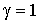 это выражение равно нулю, в чем можно убедиться устремив это выражение равно нулю, в чем можно убедиться устремив 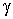 к единице и раскрыв неопределенность. При к единице и раскрыв неопределенность. При 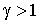 это выражение становится положительным, так как при увеличении параметра это выражение становится положительным, так как при увеличении параметра 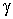 второе слагаемое в этой формуле растёт быстрее, чем убывает первое. второе слагаемое в этой формуле растёт быстрее, чем убывает первое.
|